【期刊信息】
Message刊名:石油和化工设备
曾用名:化工设备与防腐蚀
主办:中国化工机械动力技术协会
主管:中国石油和化学工业联合会
ISSN:1674-8980
CN:11-5253/TQ
语言:中文
周期:月刊
影响因子:0.185185
被引频次:8571
数据库收录:
CA 化学文摘(美)(2014);期刊分类:矿产开采
高中化学:化工流程题解法总结!收藏!
作者:网站采编
关键词:

高中化学:化工流程题解法总结!收藏!
知识归纳
无机化工流程题的特点:
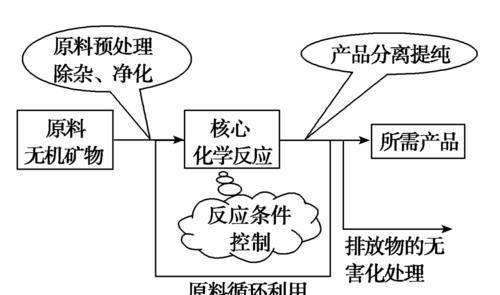
规律:主线主产品、分支副产品、回头为循环。
核心考点:物质的分离操作、除杂试剂的选择、生产条件的控制。
1. 流程的呈现主要有以物质转化为主线,以操作过程为主线,甚至有时候会以设备为主线。
2. 这类题常围绕以下几个知识点进行设问:
⑴ 反应速率与平衡理论的运用
反应物颗粒大小:反应速率、原料的利用率等
温度:反应速率、物质的稳定性、物质的结晶等
⑵ 氧化还原反应的判断、化学方程式或离子方程式的书写;
⑶ 利用控制pH分离除杂;
⑷ 化学反应的能量变化;
⑸ 实验基本操作:除杂、分离、检验、洗涤、干燥等;
⑹ 流程中的物质转化和循环,资源的回收和利用;
⑺ 环境保护与绿色化学评价。
一、原料处理的方法和作用
对原料进行预处理的常用方法及其作用:
1. 粉碎、研磨:减小固体的颗粒度,增大固体与液体或气体间的接触面积,加快反应速率。
2. 水浸:与水接触反应或溶解。
3. 酸浸:通常用酸溶,如用硫酸、盐酸、浓硫酸等,与酸接触反应或溶解,使可溶性金属离子进入溶液,不溶物通过过滤除去。近年来,在高考题出现了“浸出”操作。在化工生产题中,矿物原料“浸出”的任务是选择适当的溶剂,使矿物原料中的有用组分或有害杂质选择性地溶解,使其转入溶液中,达到有用组分与有害杂质或与脉石组分相分离的目的。
4. 浸出率:固体溶解后,离子在溶液中含量的多少(更多转化)。
5. 灼烧:除去可燃性杂质或使原料初步转化,如从海带中提取碘时的灼烧就是为了除去可燃性杂质,将有机碘转化为碘盐。
6. 灼烧、焙烧、煅烧:改变结构和组成,使一些物质能溶解;并使一些杂质在高温下氧化、分解,如煅烧高岭土和石灰石。
二、掌握核心化学反应
1. 元素及其化合物知识:化工生产将原料转变成产品的过程,也是物质经历相互转化的过程。理解物质之间的转化关系,就要用到元素及其化合物的相关知识。一般围绕铁、铜、铝、镁、氯、硫、磷、硅等元素的单质或化合物的工业制备来进行命题,需要掌握这些元素及其化合物的知识
2. 还要掌握有关化工生产的知识,熟悉的有纯碱工业、氨工业、硅单质的制备、氯碱工业、海水中提取镁、海水中提取溴等;
3. 化学反应原理:化工生产中把原料转变成产品的过程就是化学反应的过程,从化学反应原理的角度选择原料、控制条件和选择设备等,是化工生产的基本思路。化学反应原理的相关知识包括质量守恒定律、化学反应速率、化学平衡、电化学、化学热力学等,做到能综合运用这些知识分析化工生产中化学反应的情况。
① 调节溶液的pH值:使某些离子转变为沉淀而达到分离的目的,抑制某些离子的水解,防止某些离子的氧化等。在题目中常以表格形式给出信息。
例如:已知下列物质开始沉淀和沉淀完全时的pH如下表所示
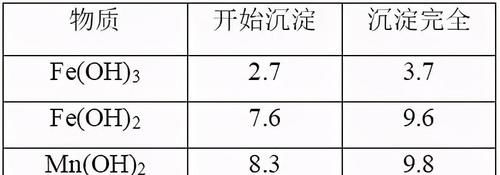
若要除去Mn2+溶液中含有的Fe2+,应该怎样做?
提示:先用氧化剂把Fe2+氧化为Fe3+,再调溶液的pH到3.7。
调节pH所需的物质一般应满足两点:
能与H+反应,使溶液pH值增大;不引入新杂质。例如:若要除去Cu2+溶液中混有的Fe3+,可加入CuO、Cu(OH)2、Cu2(OH)2CO3等物质来调节溶液的pH值。
调节溶液的pH:“酸作用还可以除去氧化物(膜);“碱作用”还可以除去油污、除去铝片氧化物、溶解铝、二氧化硅。
② 控制体系的温度
a.控制低温:防止物质的分解,如NaHCO3、NH4HCO3、H2O2、HNO3(浓)等;防止物质的挥发,如盐酸、醋酸等;抑制物质的水解,如冰水洗涤,以防止洗涤过程中的溶解损耗;增大气体反应物的溶解度,使其被充分吸收;
b.采取加热:加速某固体的溶解,加快反应速率;减少气体生成物的溶解并使其逸出;使平衡向需要的方向移动;趁热过滤,防止某物质降温时因析出而损耗或带入新的杂质;
c.控制范围:确保催化剂的催化效果,兼顾速率和转化率,追求更好的经济效益,防止副反应发生等。
三、 明确反应原理
文章来源:《石油和化工设备》 网址: http://www.syhhgsb.cn/zonghexinwen/2021/0320/723.html
投稿电话: 投稿邮箱:



